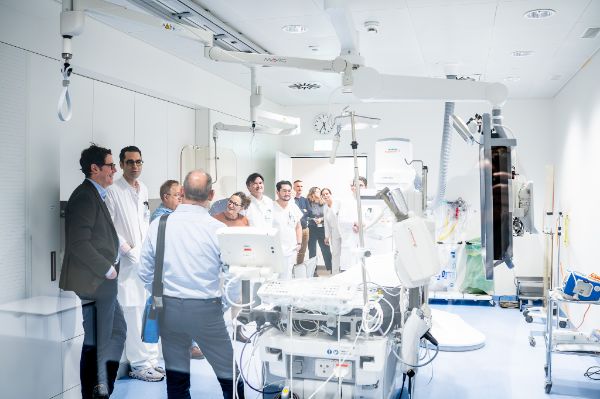
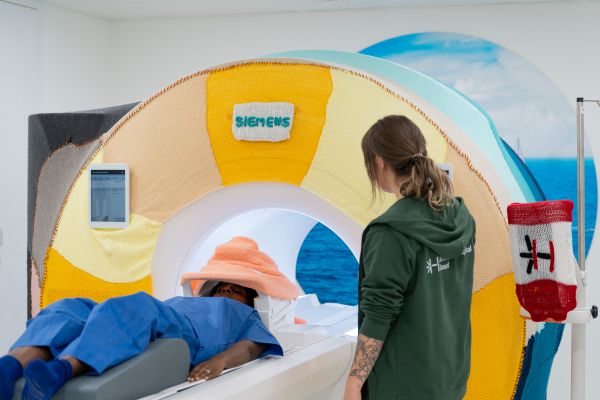
Forschung und Innovation am Unispital Basel
Wir betreiben Forschung und Innovation, damit unsere Patientinnen und Patienten vom steten Fortschritt der Medizin profitieren können. Für Ihr Wohl bilden wir eine Brücke von der Wissenschaft zum Spitalbett, damit die neuesten Forschungserkenntnisse schnell und sinnvoll in der Behandlung integriert werden. Als Patientin oder Patient können Sie uns aktiv in der Forschung unterstützen, indem Sie an aktuellen Studien teilnehmen. Mehr dazu erfahren Sie im Beitrag Teilhabe an der Forschung.
Einblicke in die USB-Forschung
Klicken Sie auf die Titel, um die Videos zu sehen.
Darmflora und Multiple Sklerose
Nasenscheidewand mit köpereigenem Gewebe reparieren
Riechtherapie bei Adipositas
Klicken Sie auf die Titel, um die Videos zu sehen.
Darmflora und Multiple Sklerose
Nasenscheidewand mit köpereigenem Gewebe reparieren
Riechtherapie bei Adipositas
Spitzenforschung in Zusammenarbeit mit der Universität Basel
Rund 600 medizinische Führungskräfte des Unispitals sind gleichzeitig Forschende und Lehrkräfte an der Medizinischen Fakultät der Universität Basel. Sie sind sowohl in der Klinik als auch in universitären Forschungsgruppen tätig, die in sieben Forschungsdepartemente organisiert sind und mit ihrer Arbeit internationale Strahlkraft erzielen.
229
Forschungsgruppen
260
Forschungsprojekte
307
laufende klinische Studien
600
Forschende und Lehrkräfte an der Medizinischen Fakultät der Universität Basel
Sieben Forschungsdepartemente
Das Universitätsspital Basel arbeitet in Forschung und Lehre eng mit der Medizinischen Fakultät der Universität Basel zusammen.Die Forschungsgruppen sind in Forschungsdepartmenten organisiert. Mehr Informationen finden Sie auf den Seiten der Forschungsdepartemente.
Das Universitätsspital Basel hat sieben Schwerpunkte in Klinik, Forschung und Entwicklung definiert, von denen sich renommierte Expertinnen und Experten bedeutende Fortschritte für die Zukunft der Medizin versprechen.
.jpg)
Am Unispital Basel werden neue Technologien wie mobilen Sensoren auf ihren Nutzen für die Gesundheitswesen geprüft. Das Innovation Management Team testet und validiert innovative Entwicklungen mit dem Ziel, sie bei der der Behandlung von Patientinnen und Patienten und zur Prävention von Erkrankungen zu nutzen.

Neues aus der Forschung am Unispital Basel
eduroam – weltweiter kostenloser WLAN Zugang
eduroam ist ein weltweites Netzwerk, das Angehörigen von Forschungs- und Bildungseinrichtungen den Internetzugang auf dem jeweiligen Campus (weltweit) ermöglicht. Auch die Mitarbeitenden des USB können diesen Dienst nutzen - am USB und weltweit.
Auf dieser Seite finden Sie Informationen und Anleitungen dafür, wie Sie den eduroam-Zugang auf Ihrem persönlichen Gerät installieren.
Bitte wählen Sie die Anleitungen (jeweils zu Installation oder Passwortwechsel) danach aus, welches Betriebssystem Sie für Ihre mobilen Geräte nutzen.
Android
macOS
Linux
Windows


.jpg)








.jpg/jcr:content/Pathologie_Hemmi-Preis%202025%20(1).jpg)
-(800-x-533-px)-(3).png/jcr:content/003000%20(1920%20x%20540%20px)%20(800%20x%20533%20px)%20(3).png)
-(800-x-533-px)-(1).png/jcr:content/003000%20(1920%20x%20540%20px)%20(800%20x%20533%20px)%20(1).png)
-(800-x-533-px).png/jcr:content/003000%20(1920%20x%20540%20px)%20(800%20x%20533%20px).png)